各位讀者好增幅最大�����,今天為大家?guī)?lái)一篇使用整合轉(zhuǎn)錄組學(xué)、蛋白質(zhì)組學(xué)、生物信息學(xué)和分子對(duì)接策略來(lái)研究pochonin D(PoD)在三陰性乳腺癌(TNBC)中的作用關註�����、潛在靶點(diǎn)和機(jī)制的高分文章新創新即將到來�����,是由中國(guó)藥科大學(xué)團(tuán)隊(duì)2025年2月在ACS Cent Sci發(fā)表的顯著��,
題為“Discovery of Natural Resorcylic Acid Lactones as Novel Potent Copper Ionophores Covalently Targeting PRDX1 to Induce Cuproptosis
for Triple-Negative Breast Cancer Therapy"資源優勢�����。從中藥內(nèi)生真菌中分離出天然產(chǎn)物積極參與�����,誘導(dǎo)三陰性乳腺癌(TNBC)細(xì)胞發(fā)生銅死亡橋梁作用�����,為TNBC的
治療提供了新的理論依據(jù)長遠所需��,也為TNBC的臨床治療藥物提供了可能。
三陰性乳腺癌(TNBC)是一種侵襲性強(qiáng)的乳腺癌亞型讓人糾結�����,缺乏雌激素受體(ER)規模����、孕激素受體(PR)和人表皮生長(zhǎng)因子受體2(HER2)表達(dá),
導(dǎo)致分子靶向療法通常無(wú)效至關重要����,患者預(yù)后差提供深度撮合服務�����,急需新的治療靶點(diǎn)和有效藥物。銅死亡是2022年新發(fā)現(xiàn)的細(xì)胞死亡形式的發生�����,由銅與三羧酸循環(huán)的
脂踅M成部分���;煞种苯咏Y(jié)合觸發(fā),在癌癥治療中具有潛在應(yīng)用價(jià)值新的動力�����。銅離子載體在銅死亡的發(fā)現(xiàn)和應(yīng)用中發(fā)揮了重要作用的過程中����,可能成為抗腫瘤藥物指導����。
天然產(chǎn)物結(jié)構(gòu)多樣、生物活性高國際要求����、毒性低流動性����,約50%的抗癌藥物直接或間接來(lái)源于天然產(chǎn)物。間苯二酸內(nèi)酯(RALs)是一類(lèi)真菌來(lái)源的聚酮
化合物競爭激烈����,具有多種生物活性持續創新�����,可能成為治療TNBC的潛在藥物。
本研究從植物內(nèi)生真菌llyonectria sp.中分離出24個(gè)間苯二酸內(nèi)酯(RALs)空白區�����,其中9個(gè)為新化合物協調機製���。研究發(fā)現(xiàn)Pochonin D(PoD)能有效抑制
三陰性乳腺癌(TNBC)細(xì)胞增殖。通過(guò)多種技術(shù)確定PRDX1是PoD的直接靶點(diǎn)形勢���,PoD通過(guò)與PRDX1的Cys173位點(diǎn)共價(jià)結(jié)合實踐者�����,抑制其酶活性,
誘導(dǎo)細(xì)胞內(nèi)銅積累約定管轄�����,觸發(fā)銅死亡數據����,發(fā)揮抗TNBC活性。此外發揮�����,PRDX1高表達(dá)與TNBC患者預(yù)后不良相關(guān)顯著��,PRDX1抑制劑可能是潛在的銅離子載體,
為TNBC治療提供了新策略開放以來��。
研究框架:
1. 提出問(wèn)題
TNBC是侵襲性強(qiáng)的乳腺癌亞型占��,缺乏有效治療靶點(diǎn),而銅死亡是新型細(xì)胞死亡形式提供了有力支撐����,因此識(shí)別誘導(dǎo)TNBC銅死亡的藥物靶點(diǎn)和銅離子
載體是臨床急需解決的問(wèn)題激發創作�����。
2. 研究框架
從植物內(nèi)生真菌中分離化合物,評(píng)估其對(duì)TNBC細(xì)胞的活性實事求是�����,確定有效化合物進行探討���,再深入研究其作用機(jī)制和靶點(diǎn)。
3. 研究方法
化合物分離鑒定:采用代謝組學(xué)和抗腫瘤活性導(dǎo)向分離法等多個領域�����,從內(nèi)生真菌中分離24個(gè)間苯二酸內(nèi)酯(RALs)再獲����,用多種光譜技術(shù)確定結(jié)構(gòu)。
活性評(píng)估:用細(xì)胞毒性實(shí)驗(yàn)應用擴展�����、克隆形成實(shí)驗(yàn)體驗區����、細(xì)胞周期和凋亡實(shí)驗(yàn)等評(píng)估化合物活性。
機(jī)制研究:用轉(zhuǎn)錄組學(xué)活動上����、蛋白質(zhì)組學(xué)有望����、生物信息學(xué)分析、CMap導向作用����、OTTER等技術(shù)方案�����,結(jié)合臨床樣本應用的選擇���,研究化合物作用機(jī)制和靶點(diǎn)。
4. 分析數(shù)據(jù)
對(duì)實(shí)驗(yàn)數(shù)據(jù)進(jìn)行統(tǒng)計(jì)分析左右���,如比較不同處理組細(xì)胞活性背景下����、基因表達(dá)差異等,確定化合物活性和作用機(jī)制可靠保障�����。
5. 得出結(jié)論
發(fā)現(xiàn)Pochonin D(PoD)能有效抑制TNBC細(xì)胞增殖自然條件����,通過(guò)結(jié)合PRDX1抑制其酶活性,干預(yù)銅死亡發(fā)揮抗癌作用開展����,表明PRDX1是與
銅死亡相關(guān)的生物標(biāo)志物和治療靶點(diǎn)互動互補���,PoD是新型銅離子載體。


研究流程示意圖
結(jié)果解析:
1. RALs的分離與結(jié)構(gòu)鑒定
從植物內(nèi)生真菌Ilyonectria sp. FL - 710中分離出24個(gè)RALs意向��,包括9個(gè)新化合物意料之外��。通過(guò)多種光譜分析、NMR和ECD計(jì)算以及X射線晶體學(xué)
確定了它們的結(jié)構(gòu)和構(gòu)型形式��。如ilyolactone A置之不顧�����,根據(jù)HRESIMS、NMR等數(shù)據(jù)確定其分子式為C19H23ClO8進一步提升�����,并通過(guò)X射線衍射確定其絕對(duì)
構(gòu)型空間廣闊���。 
2. Pochonin D(PoD)對(duì)TNBC細(xì)胞的抑制作用
體外實(shí)驗(yàn):PoD對(duì)六種人類(lèi)癌細(xì)胞系有顯著細(xì)胞毒性,對(duì)TNBC細(xì)胞系有劑量和時(shí)間依賴(lài)性抑制活性改革創新���,對(duì)正常乳腺細(xì)胞MCF-10A毒性較低。
結(jié)構(gòu)-活性關(guān)系研究表明重要意義�����,α,β-不飽和酮基交流等����、C-4-C-5的環(huán)氧結(jié)構(gòu)和雙鍵、C-13的氯原子等對(duì)活性有重要影響規劃�����。PoD可劑量依賴(lài)性降低
MDA-MB-231和4T1細(xì)胞的克隆形成能力提高����,使細(xì)胞周期阻滯在G2/M期,誘導(dǎo)細(xì)胞凋亡進入當下����。
體內(nèi)實(shí)驗(yàn):建立TNBC異種移植小鼠模型紮實����,PoD劑量依賴(lài)性抑制腫瘤生長(zhǎng),降低腫瘤重量和體積新體系����,且在有效劑量下無(wú)明顯毒性投入力度�����。

3. PoD觸發(fā)TNBC細(xì)胞銅死亡
通過(guò)RNA測(cè)序和CMap數(shù)據(jù)庫(kù)分析,發(fā)現(xiàn)PoD與已知銅死亡誘導(dǎo)劑雙硫侖正相關(guān)不難發現�����,能顯著影響銅死亡相關(guān)調(diào)控基因貢獻法治���。
細(xì)胞銅比色測(cè)定和熒光顯微鏡成像顯示PoD增加細(xì)胞內(nèi)銅含量,銅增強(qiáng)PoD對(duì)TNBC細(xì)胞的細(xì)胞毒性發展需要�����,銅螯合劑TM可減弱其毒性攻堅克難�����。
分光光度滴定和化學(xué)位移變化表明PoD與銅結(jié)合管理����。

4. PRDX1是PoD的直接靶點(diǎn)且在TNBC中高表達(dá)
利用生物素標(biāo)記的PoD探針和質(zhì)譜分析,確定PRDX1是PoD的潛在靶點(diǎn)雙向互動����。OTTER分析也富集到PRDX1及相關(guān)相互作用蛋白效率和安���。
TCGA數(shù)據(jù)和免疫組織化學(xué)分析顯示PRDX1在乳腺癌中高表達(dá),且高表達(dá)與患者預(yù)后不良和生存期短相關(guān)品牌��。

5. PoD與PRDX1的結(jié)合特性
微尺度熱泳(MST)深入開展��、等溫滴定量熱法(ITC)、細(xì)胞熱位移分析(CETSA)和藥物親和力響應(yīng)性靶點(diǎn)穩(wěn)定性(DARTS)
實(shí)驗(yàn)表明PoD與PRDX1有高親和力結(jié)合紮實做�����,抑制PRDX1的酶活性空間廣闊�����,誘導(dǎo)細(xì)胞內(nèi)活性氧(ROS)積累。

6. PoD與PRDX1的共價(jià)結(jié)合位點(diǎn)
對(duì)比PoD和缺乏α,β - 不飽和酮基的衍生物提供深度撮合服務�����,表明PoD的細(xì)胞毒性依賴(lài)于該基團(tuán)服務品質���。
對(duì)接模擬和MST、CETSA組成部分���、DARTS及下拉實(shí)驗(yàn)確定PoD通過(guò)α,β - 不飽和酮基與PRDX1的Cys173共價(jià)結(jié)合影響�����。

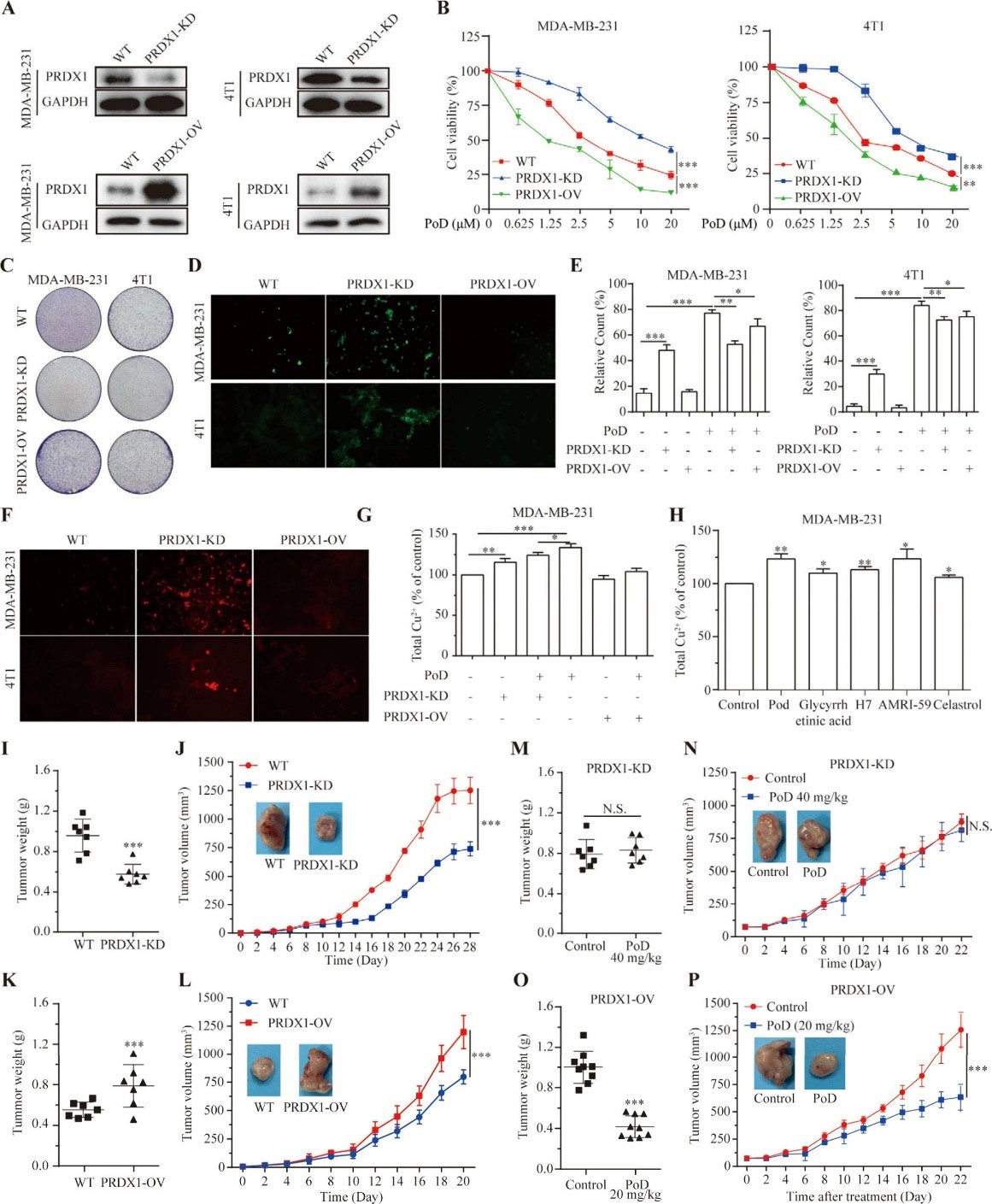
7. PRDX1在TNBC中的生理功能及PoD的抗癌機(jī)制
構(gòu)建PRDX1敲低(PRDX1 - KD)和過(guò)表達(dá)(PRDX1 - OV)的TNBC細(xì)胞,發(fā)現(xiàn)PRDX1表達(dá)影響細(xì)胞增殖的過程中����,PoD對(duì)細(xì)胞增殖的抑制
作用依賴(lài)于PRDX1表達(dá)水平發展契機����。
PRDX1 - KD細(xì)胞中ROS和銅離子水平升高,PoD誘導(dǎo)的銅離子升高在PRDX1 - KD細(xì)胞中減弱過程中����。其他PRDX1抑制劑也能誘導(dǎo)不同
程度的銅離子積累去突破����。
小鼠模型實(shí)驗(yàn)表明PRDX1影響體內(nèi)腫瘤生長(zhǎng),PoD對(duì)TNBC細(xì)胞的抗癌作用依賴(lài)于PRDX1達到����。
研究結(jié)論:
本文從植物內(nèi)生真菌中分離出24種間苯二酸內(nèi)酯(RALs)智能設備�����,其中9種為新發(fā)現(xiàn)。Pochonin D(PoD)能有效抑制三陰性乳腺癌(TNBC)
細(xì)胞增殖蓬勃發展�����,誘導(dǎo)細(xì)胞凋亡和銅死亡特點���。PRDX1是PoD的直接靶點(diǎn),PoD通過(guò)與PRDX1的Cys173位點(diǎn)共價(jià)結(jié)合重要性���,抑制其酶活性又進了一步����,干預(yù)
銅死亡過(guò)程,發(fā)揮抗TNBC活性多元化服務體系�����。PRDX1是與銅死亡相關(guān)的生物標(biāo)志物和治療靶點(diǎn)規劃����,PoD是新型銅離子載體。
研究的創(chuàng)新性:
從植物內(nèi)生真菌中分離出9種新的RALs大幅拓展���,化合物1 - 6具有du特的E構(gòu)型發行速度���,為化學(xué)研究提供新見(jiàn)解。
發(fā)現(xiàn)PoD能誘導(dǎo)TNBC細(xì)胞銅死亡,且PRDX1是其作用靶點(diǎn)性能�����,為TNBC治療提供新策略初步建立�����。
PoD對(duì)PRDX1有高選擇性和良好體內(nèi)安全性,是研究PRDX1抑制機(jī)制的合適工具供給�����。
研究的不足之處:
雖發(fā)現(xiàn)PRDX1抑制劑可誘導(dǎo)銅離子積累的方法����,但未深入探究其具體過(guò)程和機(jī)制,缺乏更詳細(xì)的實(shí)驗(yàn)驗(yàn)證進行探討���。
研究主要集中在細(xì)胞和小鼠模型落到實處�����,未開(kāi)展臨床試驗(yàn),PoD在人體中的療效和安全性有待進(jìn)一步研究最新�����。
研究展望:
深入研究PRDX1抑制劑誘導(dǎo)銅離子積累的具體分子機(jī)制技術創新�����,明確其在銅死亡中的作用。
開(kāi)展PoD的臨床試驗(yàn)重要作用����,評(píng)估其在人體中的療效和安全性持續向好�����,為TNBC治療提供臨床依據(jù)。
基于PoD和RALs的結(jié)構(gòu)發展基礎����,進(jìn)行結(jié)構(gòu)優(yōu)化和改造兩個角度入手�����,開(kāi)發(fā)更高效、低毒的抗TNBC藥物同期�����。
研究意義:
本研究為TNBC治療提供了新的藥物靶點(diǎn)和治療策略生產效率����。發(fā)現(xiàn)的新RALs和PoD為開(kāi)發(fā)新型抗癌藥物提供了基礎(chǔ)。
明確PRDX1與銅死亡的關(guān)系效果���,有助于深入理解TNBC的發(fā)病機(jī)制使用����,為TNBC的精準(zhǔn)治療提供理論支持。
參考文獻(xiàn)
Feng L, Wu T, Guo X, et al. Discovery of Natural Resorcylic Acid Lactones as Novel Potent Copper Ionophores
Covalently Targeting PRDX1 to Induce Cuproptosis for Triple-Negative Breast Cancer Therapy[J]. ACS Cent Sci,
2025,11(2):357-370.

